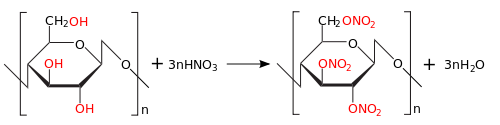- Нитроцеллюлоза
-
Нитроцеллюло́за (нитрат целлюлозы, нитроклетчатка) — групповое название химических соединений, азотнокислых сложных эфиров целлюлозы с общей формулой [C6H7O2(OH)3-x(ONO2)x] n, где х — степень замещения (этерификации), а n — степень полимеризации.
Содержание
Общие сведения
Нитроцеллюлоза — волокнистая рыхлая масса белого цвета, по внешнему виду похожа на целлюлозу. Одна из важнейших характеристик — степень замещения гидроксильных групп на нитрогруппы. В практике чаще всего применяется не прямое обозначение степени замещения, а содержание азота, выраженное в процентах по массе. В зависимости от содержания азота различают
- коллоксилин (10,7 — 12,2 % азота)
- пироксилин № 2 (12,05 — 12,4 % азота)
- пироколлодий (12,6 % азота) — особый вид нитроцеллюлозы, впервые полученный Д. И. Менделеевым, нерастворим в спирте, растворяется в смеси спирта с эфиром.
- пироксилин № 1 (13,0 — 13,5 % азота)
Плотность 1,58 — 1,65 г/см³. Степень полимеризации коллоксилина 150—600 (молекулярная масса 37500 — 150000 а. е. м.), пироксилинов 1000—2000 (молекулярная масса 250000-500000 а. е. м.). Универсальный растворитель для всех видов нитроцеллюлозы — ацетон. В воде и неполярных растворителях (бензол, четырёххлористый углерод) нитроцеллюлоза не растворяется. Растворимость н. в полярных растворителях зависит от содержания азота. В кислых и щелочных средах н. имеет низкую химическую стойкость. Температура начала разложения сухой нитроцеллюлозы 40 — 60 °C, при быстром нагреве может произойти вспышка и взрыв.История открытия
Нитроцеллюлоза — один из первых искусственных полимеров.
- 1832 — французский химик Анри Браконно (Henri Braconnot) обнаружил, что при обработке крахмала и древесных волокон азотной кислотой образуется нестойкий горючий и взрывоопасный материал, который он назвал Ксилоидин (Xyloїdine)
- 1838 — другой французский химик, Теофиль-Жуль Пелуз (Theophile-Jules Pelouze), обработал подобным образом бумагу и картон и получил похожий материал, названный им Нитрамидин (Nitramidine). Низкая стабильность полученной нитроцеллюлозы не позволяла использовать её в технических целях.
- 1846 — швейцарский химик Кристиан Фридрих Шёнбейн (Christian Fridrich Schönbein) случайно обнаружил более практичный способ получения нитроцеллюлозы. Во время работы в кухне он пролил концентрированную азотную кислоту на стол. Для удаления кислоты химик воспользовался хлопковой тряпкой, а затем повесил её сушиться на печь. После высыхания ткань сгорела со взрывом. Шёнбейн разработал первый приемлемый способ получения нитроцеллюлозы — обработкой одной части хлопковых волокон в пятнадцати частях смеси серной и азотной кислот в соотношении 50:50. Азотная кислота реагировала с целлюлозой с образованием воды и серная кислота была необходима для предотвращения разбавления. После нескольких минут обработки хлопок удалялся из кислоты, промывался в холодной воде до удаления кислот и высушивался.
- Полученный новый материал незамедлительно был применён в производстве пороха под названием ружейного хлопка (Guncotton). Нитроцеллюлоза давала в 6 раз больший объем продуктов горения, чем дымный порох, намного меньше дыма и меньше нагревала оружие. Однако производство её было крайне опасным и сопровождалось многочисленными взрывами на производствах. Дальнейшие исследования показали, что ключевую роль в опасности производства играет чистота сырья — если хлопок не был тщательно очищен и высушен, происходили внезапные взрывы.
- 1869 — в Англии под руководством Фредерика Августа Абеля (Frederick Augustus Abel) был разработана технология с измельчением нитроцеллюлозы в специальных аппаратах- голландерах и многократными (до 8 раз) длительными промывками и сушками, каждая из которых длилась до 2 суток. Соотношение серной и азотной кислот в смеси было изменено до 2:1. По такой технологии удавалось получать достаточно стабильный при хранении и применении продукт.
Получение
Лучшим сырьём для производства нитроцеллюлозы считаются длинноволокнистые сорта хлопка ручной сборки. Хлопок машинной сборки и древесная целлюлоза содержат значительное количество примесей, усложняющих подготовку и снижающих качество продукции. Нитроцеллюлозу получают действием на очищенную, разрыхлённую и высушенную целлюлозу смесью серной и азотной кислот, называемой нитрующей смесью:
Ниже приведена реакция получения тринитроцеллюлозы в лабораторных условиях:
Концентрация применяемой азотной кислоты обычно выше 77 %, а соотношение кислот и целлюлозы может быть от 30:1 до 100:1. Полученный после нитрования продукт подвергается многоступенчатой промывке, обработке слабокислыми и слабощелочными растворами, измельчению для повышения чистоты и стойкости при хранении. Сушка нитроцеллюлозы — сложный процесс, иногда совместно с сушкой применяется обезвоживание (этанолом, спирто-эфирными смесями). Практически вся нитроцеллюлоза после получения используется в производстве различных продуктов. В случае необходимости хранится во влажном состоянии с содержанием воды или спирта не ниже 20 %.
Применение
Нитроцеллюлоза производится в больших количествах во многих странах мира и находит много различных применений:
- Бездымный порох, обычно пироксилин. За более чем 100-летнюю историю развития химии и технологии предложены тысячи разнообразных составов, многие из которых производились десятками и сотнями тысяч тонн. (Баллистит, Кордит).
- Взрывчатые вещества. Нитроцеллюлоза в чистом виде из-за низкой термической стойкости не применяется, но существует неисчислимое множество реальных и фантастических взрывчатых составов с её применением. В 1885 году была впервые получена смесь нитроцеллюлозы с нитроглицерином, названная «гремучий студень».
- Ранее использовалась как подложка Фото- и киноплёнки. в связи с горючестью была вытеснена Ацетилцеллюлозой и полиэтилентерефталатом (лавсаном).
- Целлулоид. До сих пор лучшие шарики для настольного тенниса производятся из нитроцеллюлозы.
- Нитроцеллюлозные мембраны для иммобилизации белков.
- В индустрии развлечений для производства быстросгорающих предметов в реквизите артистов-фокусников.
- Нитроцеллюлозные мембраны используют для гибридизации нуклеиновых кислот, например, при Саузерн блоттинге.
См. также
Для улучшения этой статьи желательно?: - Найти и оформить в виде сносок ссылки на авторитетные источники, подтверждающие написанное.
НитратыДинитрат гидразина (N2H6(NO3)2) • Изопентилнитрат ((CH3)2CHCH2CH2ONO2) • Метилнитрат (CH3ONO2) • Нитрат актиния(III) (Ac(NO3)3) • Нитрат алюминия (Al(NO3)3) • Нитрат аммония (NH4NO3) • Нитрат бария (Ba(NO3)2) • Нитрат берилия (Be(NO3)2) • Нитрат висмута (Bi(NO3)3) • Нитрат гадолиния (Gd(NO3)3) • Нитрат гидразина (N2H5NO3) • Нитрат гидроксиламина ((NH3OH)NO3) • Нитрат гуанидина (C(NH2)3NO3) • Нитрат железа(III) (Fe(NO3)3) • Нитрат кадмия (Cd(NO3)2) • Нитрат калия (KNO3) • Нитрат кальция (Са(NО3)2) • Нитрат кобальта(II) (Co(NO3)2) • Нитрат кобальта(III) (Co(NO3)3) • Нитрат лития (LiNO3) • Нитрат магния (Mg(NO3)2) • Нитрат марганца (Mn(NO3)2) • Нитрат меди(II) (Cu(NO3)2) • Нитрат мочевины ((NH2)2CO•HNO3) • Нитрат натрия (NaNO3) • Нитрат неодима (Nd(NO3)3) • Нитрат никеля(II) (Ni(NO3)2) • Нитрат палладия(II) (Pd(NO3)3) • Нитрат ртути(I) (Hg2(NO3)2) • Нитрат ртути(II) (Hg(NO3)2) • Нитрат рубидия (RbNO3) • Нитрат свинца(II) (Pb(NO3)2) • Нитрат серебра(I) (AgNO3) • Нитрат скандия(III) (Sc(NO3)3) • Нитрат стронция (Sr(NO3)2) • Нитрат урана (U(NO3)2) • Нитрат уранила (UO2(NO3)2) • Нитрат хлорина (ClONO3) • Нитрат хрома (Cr(NO3)3) • Нитрат цезия (CsNO3) • Нитрат цинка (Zn(NO3)2) • Нитраты целлюлозы ([C6H7O2(OH)3-x(ONO2)x]n) • Нитроглицерин (O2NOCH(CH2ONO2)2) • Пропилнитрат (C3H7ONO2) • Церий-аммоний нитрат ((NH4)2Ce(NO3)6) • Этилнитрат (C2H5ONO2)
 Категории:
Категории:- Нитраты
- Взрывчатые вещества
- Нитросоединения
Wikimedia Foundation. 2010.